全国白癜风爱心大使 https://m.39.net/disease/a_6205157.html
三维(three―dimentional,3D)打印也称为“增材制造”或“快速成型”技术,医学3D打印,即以电子计算机断层扫描(CT)、核磁共振(MRI)、超声等影像资料为源数据,构建目标结构的3D模型文件,通过打印软件设定相关的打印参数,为每个打印层次生成轮廓和填充路径,进而指导3D打印机采用不同的打印方式构建目标结构的实体模型。基于心脏增强CT数据,应用开源软件进行建模,并应用国产的赛纳数字医疗3D打印机对多例复杂先天性心脏病(先心病)患者的心脏结构进行打印。本研究对这些3D打印模型的精确性进行评估。
资料和方法
年4月至年6月,医院应用双源CT机(SomatomDefinitionFlash,Siemens,德国)对50例复杂先心病患者进行心脏增强CT扫描,采用前瞻性心电门控技术获取收缩期图像,层厚0.75him,扫描范围自胸廓入口至右膈下5CITI水平。基于获取的DICOM数据,应用开源软件(3DSlicer)进行3D建模,表面进行平滑处理,输出3D数字模型(stereo―lithographic,stl)到国产3D打印机(JPro,珠海赛纳,中国)进行打印,打印技术是直喷式彩色多材料的WJP白墨填充技术(White―Jet―Process)。
全组男22例,女28例;年龄1个月~61岁,中位年龄24个月。肺动脉闭锁11例、单心室和冠状动脉起源异常各4例,右心室双出口、法洛四联症、完全性肺静脉异位引流和双主动脉弓各3例,主动脉缩窄和/或弓发育不良、肺动脉狭窄、肺动脉吊带、共同动脉干和体静脉异位引流各2例,完全性大动脉转位、冠状动脉心室瘘、室间隔缺损合并右心室双腔、主动脉弓离断、左心室流出道梗阻、部分型肺静脉异位引流、肺动脉狭窄合并肺静脉狭窄、部分型心内膜垫缺损和冠状动脉.肺动脉瘘各1例。其中8例有心血管手术史。1例单心室/三尖瓣闭锁合并大动脉转位和室间隔缺损的患者经全科讨论后建议出院继续观察,择期行Glenn手术;1例肺动脉闭锁合并室间隔缺损患者和1例主动脉缩窄合并肺动脉狭窄的患者因家庭原因放弃手术并签字出院。其他47例均接受手术治疗,其中45例术后顺利出院。l例主动脉缩窄合并弓发育不良患者因低心排血量综合征死亡,1例肺动脉闭锁合并室间隔缺损患者术后因肺气肿合并呼吸衰竭死亡。
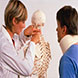
每例患者选择3个测量位点(共个),根据病例特点及测量可行性,选择测量的位点包括主动脉弓横径、降主动脉横径、锁骨下动脉主动脉端横径、室间隔缺损直径、左/右心室流出道横径、肺动脉起始部横径、左/右肺动脉横径、主一肺动脉侧支血管横径等。放大CT图像后应用线性测量工具进行测量,并在打印模型上应用游标卡尺进行测量(图1)。分别测量两次,取平均数。应用SPSS24.0统计软件进行分析。计量数据以置±S表示,分类数据表示为频率或百分比。计算CT.模型测量值的Pearson相关系数。利用D检验(Kolmogorov―Smirnov检验)和Q―Q图对CT一模型测量值的差值进行分析,以评估其分布的正态性。采用配对t检验和Bland.Altman分析比较CT一模型测量值,P0.05为差异有统计学意义。
结果
cT一模型测量值Pearson相关系数0.,两组数据有极强相关性。CT一模型测量值的差值(一0.07±0.67)mm,D检验P=0.2,且Q.Q图(图2)显示数据点与理论直线重合度较高,两组数据的差值符合正态分布;配对t检验P=0.,两组数据差异无统计学意义。Bland.AItman分析差值的一致性界值区间(X一1.96S,X+1.96S)为(一1.29ITlm,1.16mill),Bland.Altman散点图(图3)个点中个(95.33%)在一致性界值区间内。
讨论
我们应用国产3D打印机打印50例复杂先心病患者的心血管结构,结果显示,在将二维图像转化为三维实体模型的过程中,没有产生过多的误差,较完整地保留cT数据的信息量。已有多项相关研究报道了3D打印技术具有辅助先心病诊疗的作用。1―2I,而3D打印的精确性是发挥作用的重要基础。不同的打印方式的精确度不尽相同,3D打印的方式可以分为熔积成型、材料喷射、立体光固化成型、黏结剂喷射和选择性激光烧结等Ⅲ。。文献报道应用的打印方式集中在熔积成型,且均为单色打印∞4‘5’卜“。11J,我们应用的是直喷式彩色多材料的WJP白墨填充技术(White.Jet.Process),属于改良的光固化成型技术,其技术原理是喷射超薄层的光敏树脂,并且可以喷射多种不同的材料,其最薄层仅16“m(0.mm),表面光滑、细节丰富、可以彩色成型。我们的研究中模型不同的心血管结构采用了不同的颜色打印,方便医师观察。Valverde等报道打印模型与影像数据的差值均值是(一0.12±1.40)lllm∞o和(0.27±0.73)lioj,前者差异性较大,后者13例(13/40)因机器问题需要再次打印。Olejnik等。9。报道模型与影像数据的差值均值(0.19±0.38)nlm,但仅测量32个位点,统计学意义不充分。我们的研究中打印模型均一次成功,共测定个位点,打印模型与影像数据差值P=0.2,结合Pearson系数及Bland―Altman散点图的结果,统计学上认为两组数据具有高度的一致性,即模型精准度高。我们应用的3D打印机的喷射层厚仅0.mm,低于CT扫描层厚0.75mm,因此打印精度高于CT扫描的图像。除测量误差外,其他导致误差的可能原因是,CT图像上不能完全辨认清楚血管壁和心室壁等结构,只能通过局部辨认清楚的部分推测其余部分,而且建模过程中必须对3D数字模型进行表面光滑处理,这些步骤分区会影响建模的准确性。相比于熔积成型,光固化打印模型的不足是硬度不强,但是通过改进材料,我们打印的模型不易碎,而且具有一定的柔软性,完全能够满足临床的需求。随着未来更多的物理学性能改进,模型的用途具有广阔的可能性,例如进行更多的模拟操作和血流动力学分析等。
综上,基于心脏增强cT数据的3D建模、应用赛纳数字医疗国产3D打印机打印的心脏模型能完整保留cT数据信息,具有良好的精确性,可以直观准确地再现心脏结构,帮助临床诊疗。
图1复杂先心病患儿心血管结构3D打印位点测量,左图为线性工具测量cT图像位点;右图为游标卡尺测量3D打印模型位点



 当前时间:
当前时间:  E-Mail:
E-Mail: